La datación radiométrica, la datación radiactiva o la datación por radioisótopos es una técnica que se utiliza para fechar materiales como rocas o carbono, en los que se incorporaron selectivamente trazas de impurezas radiactivas cuando se formaron.
El método compara la abundancia de un isótopo radiactivo natural dentro del material con la abundancia de sus productos de desintegración, que se forman a una tasa de desintegración constante conocida.
El uso de la datación radiométrica fue publicado por primera vez en 1907 por Bertram Boltwood y ahora es la principal fuente de información sobre la edad absoluta de las rocas y otras características geológicas, incluida la edad de las formas de vida fosilizadas o la edad de la Tierra misma y también se puede utilizar para fechar una amplia gama de materiales naturales y artificiales.
Junto con los principios estratigráficos, los métodos de datación radiométrica se utilizan en geocronología para establecer la escala de tiempo geológico. Entre las técnicas más conocidas se encuentran la datación por radiocarbono, la datación por potasio-argón y la datación por uranio-plomo.
Al permitir el establecimiento de escalas de tiempo geológicas, proporciona una importante fuente de información sobre las edades de los fósiles y las tasas deducidas de cambio evolutivo.
Los diferentes métodos de datación radiométrica varían en la escala de tiempo en la que son precisos y en los materiales a los que se pueden aplicar.
Generalidades
Los átomos están conformados por un núcleo, que contiene protones y neutrones. Alrededor del núcleo orbitan los electrones que tienen una carga eléctrica negativa. Los protones, por otro lado, tienen una carga positiva.
Un neutrón es en realidad una combinación de un protón y un electrón, pues no tiene carga (es neutro).
El número atómico (el número que identifica cada elemento) es el número de protones que tiene en su núcleo.
Cada elemento tiene un número diferente de protones y, por tanto, un número atómico diferente (hidrógeno = 1, carbono = 6, oxígeno = 8, uranio = 92, etc.).
Los átomos de un mismo elemento tienen siempre el mismo número de protones, de manera que el número atómico se mantiene constante.
Prácticamente toda la masa de un átomo (99,9 por ciento) se encuentra en el núcleo, lo que indica que los electrones no tienen prácticamente masa.
Así pues, sumando los protones y los neutrones del núcleo de un átomo obtenemos el número másico del átomo.
El número de neutrones puede variar, y esas variantes, o isótopos, tienen diferentes números másicos.
Para resumir con un ejemplo, el núcleo del uranio tiene siempre 92 protones, de manera que su número atómico es siempre 92. Pero su población de neutrones varía, de modo que el uranio tiene tres isótopos: uranio-234 (protones + neutrones = 234), uranio-235 y uranio-238.
Todos estos isótopos están mezclados en la naturaleza. Tienen el mismo aspecto y se comportan igual en las reacciones químicas.
Fundamentos de Radiactividad
Las fuerzas que unen los protones y los neutrones en el núcleo suelen ser fuertes. Sin embargo, en algunos isótopos, los núcleos son inestables porque las fuerzas que unen los protones y los neutrones no son lo bastante fuertes.
Como consecuencia, los núcleos se descomponen, o desintegran, espontáneamente en un proceso denominado radiactividad.
¿Qué ocurre cuando se descomponen los núcleos inestables?
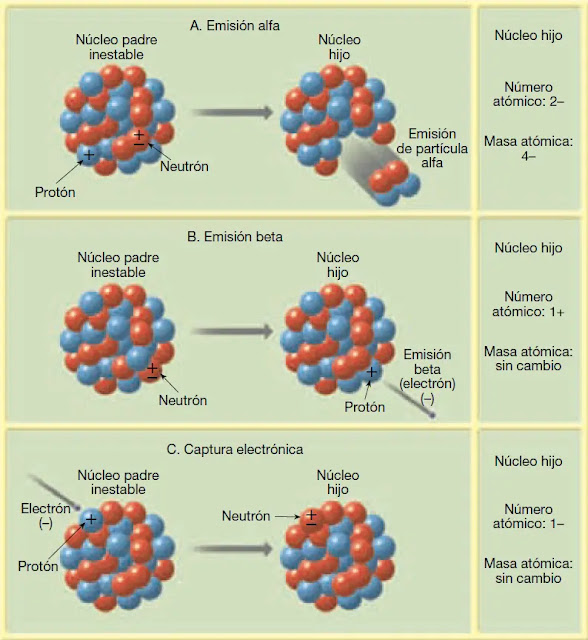
En la Figura 1, se ilustran tres tipos comunes de desintegración radiactiva, que pueden resumirse como sigue:
- Pueden emitirse partículas alfa (partículas α) del núcleo. Una partícula alfa está compuesta por dos protones y dos neutrones. Por tanto, la emisión de una partícula alfa significa que el número másico del isótopo se reduce en 4 y el número atómico, en 2.
- Cuando se expulsa una partícula beta (partícula β), o electrón, de un núcleo, el número másico se mantiene inalterado, porque los electrones prácticamente no tienen masa. Sin embargo, dado que los electrones proceden de un neutrón (recordemos que un neutrón es una combinación de un protón y un electrón), el núcleo contiene un protón más que antes. Por consiguiente, el número atómico aumenta en
- A veces un electrón es capturado por el núcleo. El electrón se combina con un protón y forma un neutrón. Como en el último ejemplo, el número másico se mantiene invariable. Sin embargo, dado que el núcleo contiene ahora un protón menos, el número atómico disminuye en 1.
Se denomina padre al isótopo radiactivo inestable e hijos a los isótopos que resultan de su desintegración.
Cuando el radioisótopo padre, como el uranio-238 (número atómico 92, número másico 238), se descompone, sigue una serie de etapas, emitiendo 8 partículas alfa y 6 partículas beta antes de convertirse finalmente en el isótopo hijo estable, el plomo-206 (número atómico 82, número másico 206). Uno de los radioisótopos hijo producidos durante esta serie de descomposición es el radón.
Período de Semidesintegración
El tiempo necesario para que se desintegre la mitad de los núcleos de una muestra se denomina período de semidesintegración del isótopo. El período de semidesintegración es una forma común de expresar la velocidad de desintegración radiactiva.
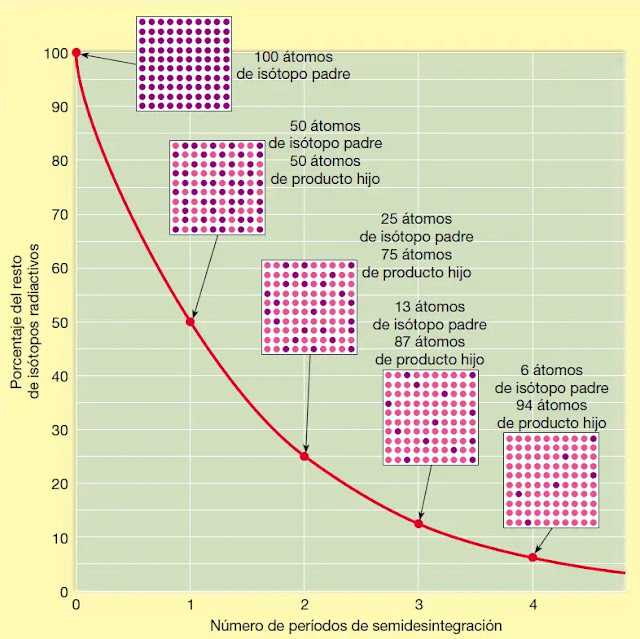
En la Figura 2 se ilustra lo que ocurre cuando un radioisótopo padre se descompone directamente en el isótopo hijo estable. Cuando las cantidades del padre y del hijo son iguales (proporción 1/1), sabemos que ha transcurrido un período de semidesintegración.
Cuando queda una cuarta parte de los átomos del radioisótopo padre original y las tres cuartas partes se han desintegrado para producir el isótopo hijo, la proporción padre/hijo es 1/3 y sabemos que han transcurrido dos vidas medias.
Después de tres vidas medias, la proporción de átomos del padre a átomos del hijo es de 1/7 (un átomo padre por cada siete átomos hijos).
Si se conoce el período de semidesintegración de un isótopo radiactivo y puede determinarse la proporción padre/hijo, puede calcularse la edad de la muestra.
Por ejemplo, supongamos que el período de semidesintegración de un isótopo inestable hipotético es de un millón de años y la proporción padre/hijo de la muestra es 1/15, dicha proporción indica que han transcurrido cuatro períodos de semidesintegración y que la muestra debe tener 4 millones de años.
¿Es fiable la datación radiométrica?
¡La respuesta es SI! Las velocidades de desintegración de muchos isótopos se han medido con precisión y no varían bajo las condiciones físicas que existen en las capas externas de la Tierra.
Por consiguiente, cada isótopo radiactivo utilizado para datación ha estado desintegrándose a una velocidad fija desde la formación de las rocas en las que aparece, y los productos de su descomposición se han estado acumulando a una velocidad equivalente.
Por ejemplo, cuando el uranio se incorpora en un mineral que cristaliza a partir de un magma, no existe plomo (el isótopo hijo estable) procedente de una desintegración previa. El «reloj» de la datación radiométrica empieza en ese momento.
A medida que se desintegra el uranio de ese mineral recién formado, van quedando atrapados los átomos del producto hijo y acaban acumulándose cantidades medibles de plomo.
Efectos de contaminación
La ecuación básica de la datación radiométrica requiere que ni el isótopo padre ni el producto hijo puedan entrar o salir del material después de su formación.
Deben considerarse los posibles efectos de confusión de la contaminación de los isótopos padre e hijo, al igual que los efectos de cualquier pérdida o ganancia de dichos isótopos desde que se creó la muestra.
Por lo tanto, es esencial tener la mayor información posible sobre el material que se está fechando y verificar posibles signos de alteración. La precisión se mejora si se toman medidas en múltiples muestras de diferentes ubicaciones del cuerpo rocoso.
Alternativamente, si se pueden fechar varios minerales diferentes de la misma muestra y se supone que se formaron por el mismo evento y estaban en equilibrio con el yacimiento cuando se formaron, deberían formar una isócrona.
Esto puede reducir el problema de la contaminación. En la datación con uranio-plomo, se utiliza el diagrama de concordia, que también disminuye el problema de la pérdida de isótopos.
Finalmente, puede ser necesaria la correlación entre diferentes métodos de datación para confirmar la edad de una muestra.
Por ejemplo, la edad de los gneises Amitsoq del oeste de Groenlandia se determinó en 3,60 ± 0,05 Ga (hace mil millones de años) utilizando la datación con uranio-plomo y 3,56 ± 0,10 Ga (hace mil millones de años) utilizando la datación radiométrica con plomo-plomo, resultados que son consistentes entre sí.
La datación radiométrica precisa generalmente requiere que el padre tenga una vida media lo suficientemente larga como para que esté presente en cantidades significativas en el momento de la medición, la vida media del padre se conoce con precisión y se produce suficiente producto hijo para medirlo con precisión y distinguirlo de la cantidad inicial del producto hijo presente en el material.
Los procedimientos utilizados para aislar y analizar los isótopos padre e hijo deben ser precisos y exactos. Esto normalmente implica espectrometría de masas de relación isotópica.
La precisión de un método de datación depende en parte de la vida media del isótopo radiactivo involucrado. Por ejemplo, el carbono-14 tiene una vida media de 5.730 años.
Después de que un organismo ha estado muerto durante 60.000 años, queda tan poco carbono-14 que no se puede establecer una fecha exacta.
Por otro lado, la concentración de carbono-14 cae tan abruptamente que la edad de los restos relativamente jóvenes se puede determinar con precisión en unas pocas décadas.
Fuente:
- Tarbuck, E. y Lutgens, F. Ciencias de la Tierra 8va. Edición. Pearson Education. Madrid, España (2005).
- Colaboradores de Wikipedia. Radiometric dating. Wikipedia, la enciclopedia libre (2021). https://en.wikipedia.org/wiki/Radiometric_dating
- Las dataciones por radiocarbono. Prehistoria Viva. https://www.prehistoriaviva.es/l/las-dataciones-por-radiocarbono (2020).
Si te ha gustado este artículo y sientes que aporta valor, te invitamos a compartirlo en tus redes sociales preferidas, así nos ayudas a difundir información a todo a quien pueda interesar. Si tienes alguna duda, comentario o sugerencia, puedes dejarlo abajo en la sección de comentarios. ¡Nos interesa tu opinión!



Muy buena información, excelente para la preparación de la clase sobre está temática, lástima que no pueda acceder a las figuras, pues al intentarlo me sale un comentario que reza que mi país, Cuba, no puede acceder a las mismas ¡increíble pero cierto!
Hola Rolando, correo enviado con las figuras. Saludos y suerte!